януари 2019
-
Нови открития за връзката между вирус на Епщайн-Бар и цитомегаловирус с автоимунните заболявания
Към днешна дата се смята, че етиологията на автоимунни заболявания е многофакторна – генетична предразположеност, неправилно…
-

Имунни отговори към хранителни антигени
За да се справи с огромния брой антигени (потенциални алергени), постъпващи в гастроинтестиналния тракт, чревната лигавица…
-

Трансплантация на панкреасни островни клетки
Островните клетки на панкреаса могат да бъдат трансплантирани. Тази β – клетъчна заместителна терапия обещава да…
-

Ранна и оптимизирана диагностика на системната склероза чрез имунологични изследвания
Прогресивната системна склероза (ПСС) е най-често срещаната форма на склеродермия. Тя представлява хронично системно автоимунно забoляване.
-
Целиакия и инфертилитет
Двупосочна ли е асоциацията между целиакия и инфертилитет?
-

Стрес и автоимунни заболявания
Причините за загубата на толерантност при автоимунните болести са много – генетични, на околната среда, хормонални…
-

Нови и стари имунологични факти за тиреоидита на Хашимото
Тиреоидитът на Хашимото е част от спектъра на автоимунните заболявания на щитовидната жлеза и се характеризира…
-

Антитела срещу деамидирани глиадинови пептиди в диагностиката на целиакията
Целиакията е глобален здравен проблем с честота до 1% от общата популация и висок риск за…
-
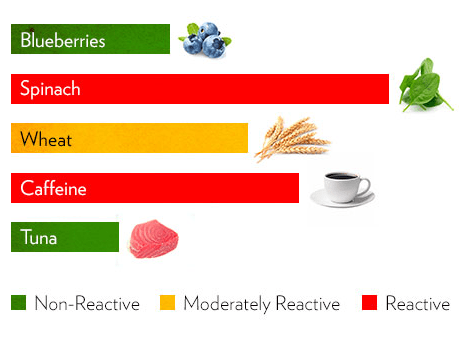
Кръвни тестове за определяне на IgG антитела при хранителна нетолерантност
Основен проблем на диагностиката на непоносимост към някои храни е, че пациентите могат да имат не…
-

Къде се намира хранителната нетолерантност в спектъра на реакции към храните?
Литературните данни показват, че около 60% от населението на света страда от непоносимост към поне един…
